九游体育app娱乐这些患者急需新的调节程序-Ninegame-九游体育(中国)官方网站|jiuyou.com
*仅供医学专科东说念主士阅读参考
乳腺癌是严重恐吓全寰宇女性健康的恶性,其中激素受体阳性/东说念主表皮滋长因子受体2阴性(HR+/HER2-)是乳腺癌最常见的亚型,约占新发乳腺癌的70%[1]。中国每年新发乳腺癌病例中,约3%~10%的妇女在确诊时即有远方挪动。早期患者中,30%可发展为晚期乳腺癌,晚期乳腺癌患者5年生计率仅为20%[2]。晚期乳腺癌是乳腺癌发展的特别阶段,在调节取舍和疗效方面均不同于乳腺癌的其他阶段。这些患者不仅要承受疾病自己的职守,还要面对款式上和经济上的巨大压力。
HR+晚期患者以内分泌调节为基石
内分泌调节是激素受体阳性(hormone receptor-positive,HR阳性)乳腺癌患者主要的全身调节技能。乳腺癌的内分泌调节资历了百年发展历史,他莫昔芬(tamoxifen,TAM)、三种常见芳醇化酶阻碍剂(aromatase inhibitors,AI)、氟维司群(fulvestrant)是乳腺癌内分泌调节的基本药物。关于HR+晚期乳腺癌的调节,国表里指南[3-4]均指出:内分泌调节是HR+晚期乳腺癌的调节基石。即使存在内脏挪动,以内分泌为基础或聚首调节还是是优选调节决策,但要吞并HR抒发气象、内分泌调节的明锐性、疾病发展速率、肿瘤负荷、体格条款等详细决定。

图1:中国抗癌协会乳腺癌诊治指南与范例 (2024简要版)

图2:2024 V4 NCCN乳腺癌指南更新
在单药内分泌调节期间,AI和氟维司群均是HR阳性HER2阴性MBC的尺度决策,关于疾病发展平缓、非内脏危象患者首选内分泌调节,临床推论中大王人内脏挪动甚而内脏危象患者禁受化疗算作肇始调节。跟着CDK4/6阻碍剂的连续上市、内分泌调节药的医保策略变化,以CDK4/6阻碍剂为基础聚首内分泌调节的决策成为一线主流。由于HR阳性患者在早期频频会禁受多种内分泌调节,因此关于晚期患者,国内指南更新遵命患者既往调节的不同而赐与分层调节策略。关于肿瘤负荷大、内脏危象的患者,Right choice接头[5]为内分泌聚首CDK4/6阻碍剂调节提供了字据。该接头是针对高侵袭性HR阳性HER2阴性MBC(内脏危象占比52.3%)一线调节的随即对照Ⅱ期接头,ER抒发≥50%阳性的患者占比85.6%,斥逐骄慢:与聚首化疗比拟,内分泌聚首CDK4/6阻碍剂权臣延迟患者的PFS(24.0 比12.3个月,HR=0.54,P=0.0007)。
谨守2024版CSCO指南[6]的分层调节策略,关于既往未经内分泌调节或者TAM调节失败的患者,不错优选AI聚首CDK4/6阻碍剂。关于HR阳性乳腺癌患者,在早期调节阶段,AI是主要的调节技能。然则,跟着调节时期的延迟,患者对AI产生耐药性的风险渐渐增多,荒谬是在晚期患者中,AI耐药的情况更为普遍。关于SAI或NSAI调节失败的患者,推选将氟维司群与CDK4/6阻碍剂的聚首疗法算作I级推选。多项接头如MONARCH 2/plus[7]说明了氟维司群与阿贝西利CDK4/6阻碍剂聚首使用在调节晚期HR阳性乳腺癌中的权臣疗效。在乳腺癌细胞中,CDK4/6阻碍剂能通过阻碍细胞周期素D1与CDK4/6激酶的吞并,阻断Rb卵白磷酸化,从而阻碍细胞周期从G1期到S期的程度,阻碍肿瘤细胞增殖,对ER阳性乳腺癌具有延松驰逆转内分泌耐药的作用[8]。
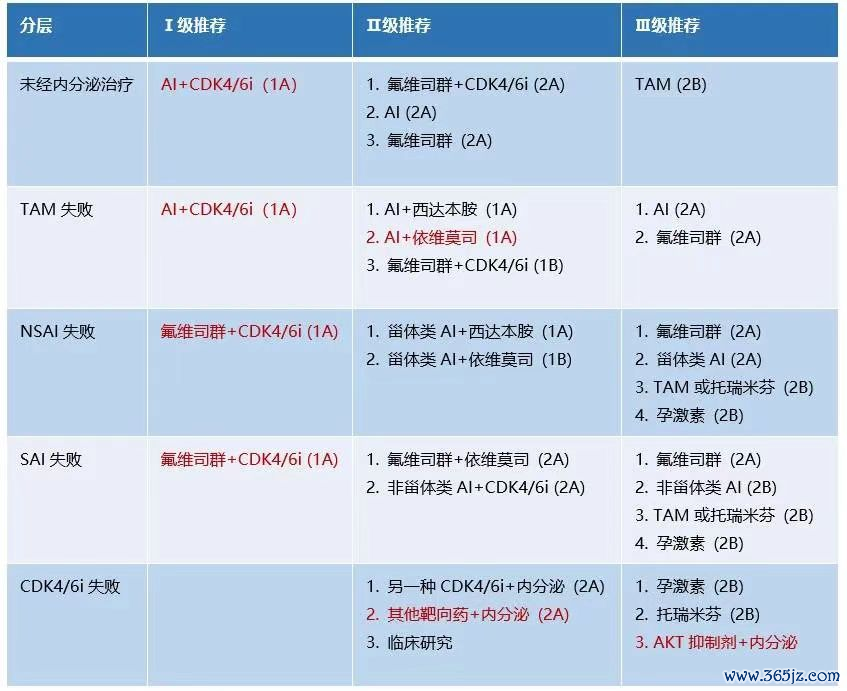
图3:2024 CSCO BC指南
新式内分泌及靶向药物的探索
关于CDK4/6阻碍剂调节失败的患者,寻找新的调节策略已成为临床使命中的迫切任务。跟着CDK4/6阻碍剂在一线、二线乃至辅助强化调节中的无边期骗,越来越多的患者面对着在长久用药后疾病再次进展的挑战。这些患者急需新的调节程序,以期粗略督察较高的生活质料并斥逐长久带瘤生计。
新式口服取舍性雌激素受体降解剂(SERD)药物的发展远景备受热心,口服SERD类药物以其私有的作用机制、安全高效的特点和浅易方便的期骗方式,平缓成为HR+乳腺癌内分泌调节的研发烧点,况兼在EMERALD[9]等系列接头中赢得了积极的斥逐,荒谬是关于佩带ESR1突变的患者[10]。晚期阶段在CDK4/6i阻碍剂失败后,口服SERD上风东说念主群的筛选,前哨与CDK4/6i聚首使用灵验性的探索,辅助阶段在高风险东说念主群中聚首或不聚首CDK4/6i,进一步裁减患者物化率,是当下口服SERD临床磨真金不怕火的热门。
现时,HR+晚期乳腺癌患者内分泌调节的另一个趋势是与靶向调节进行聚首,其效能优于单药内分泌调节。若一线调节中患者未禁受CDK4/6阻碍剂调节,二线调节患者仍然不错取舍CDK4/6阻碍剂聚首内分泌进行调节。除CDK4/6阻碍剂外,其他靶向药物也不错和内分泌调节聚首期骗。如AKT阻碍剂、PI3K阻碍剂、HDAC阻碍剂、mTOR阻碍剂、ADC药物等,正在渐渐蜕变HR+晚期乳腺癌调节方式,给患者带来更多取舍和更长的生计。
约50%HR+/HER2-乳腺癌患者存在PI3K/AKT/PTEN通路基因的突变,以PIK3CA基因为主[11];既往接头数据报说念中国东说念主群PIK3CA突变率约32%-50%[12],各人突变率31-40%[11]。与白种东说念主比拟,中国乳腺癌东说念主群的AKT1基因突变频率更高,约4-8%[12]。PAM信号通路在乳腺癌中的荒谬激活不仅是疾病进展的关节驱动成分,也与调节耐药性的变成和加重密切商酌,这种过度激活对内分泌调节、化疗以及靶向调节的耐药性产生了长远的影响。雌激素受体与雌二醇吞并后,能激活PAM通路信号,促进肿瘤细胞滋长。PAM通路也可磷酸化ER,使其在不依赖雌激素的情况下被激活,并基于细胞核进展转录作用,促进肿瘤细胞增殖。此外,PAM信号通路的激活还能颐养与该通路商酌的卵白活性,迤逦参与CDK4/6阻碍剂和抗HER2调节的耐药性变成经由,这进一步增多了乳腺癌调节的复杂性[13]。既往多项接头骄慢,与PAM通路正常的乳腺癌患者比拟,存在通路基因蜕变者肿瘤进展风险更高,DFS及OS更差。一项纳入7项接头的Meta分析骄慢,PIK3CA基因特定激活突变是乳腺癌的颓落不良预后成分(HR=1.67,p=0.007),权臣增多了疾病进展与物化风险(HR=2.05,p=0.002)[14]。因此,深入意志、准确识别、精确检测并灵验调节PAM通路商酌突变,关于训诲乳腺癌调节效能至关高大。瞻望异日,PAM通路阻碍剂将成为新的接头焦点,触及多个关节问题,如最好调节模式是序贯使用照旧聚首使用,针对耐药患者群体的调节策略,以及对通路进行精确检测的需求,这包括取舍稳妥的检测样本、细目检测时期点,以及怎么依据检测斥逐来带领药物取舍等。现在这类接头要点热心在CDK4/6i使用后,关于HR阳性晚期乳腺癌患者更多的药物取舍可能性。总之,异日在HR阳性晚期乳腺癌的调节中,将有多种新兴药物和调节策略值得热心和探索,以期为患者提供更多灵验的调节程序,改善生活质料。
此外,组卵白去乙酰化酶(HDAC)阻碍剂通过阻碍商酌 HDAC 亚型以增多染色质组卵白的乙酰化水平来激发染色质重塑,并由此产生针对肿瘤发生的多条信号传递通路基因抒发的蜕变(即表不雅遗传蜕变),粗略引导肿瘤干细胞分化、逆转肿瘤细胞的上皮间充质表型转机(EMT)等作用,进而在归附耐药肿瘤细胞对药物的明锐性和阻碍肿瘤挪动、复发等方面进展潜在作用[14]。HDAC阻碍剂在中国已有多年的临床期骗教训,在后线调节中为改善耐药性提供了新的决策。比如,西达本胺聚首依西好意思坦在绝经后HR+/HER2-ABC患者中骄慢出致密的疗效和安全性,然则HDAC阻碍剂尚未纳入医保,这在一定程度上截止了它们在临床推论中的无边期骗。
免疫调节在TNBC中势如破竹,好多中心运行在HR+ HER2-乳腺癌围术期中探索免疫调节的价值。在I-SPY2[15]的一个HR+/HER2-部队中,说明了新辅助帕博利珠单抗聚首化疗能灵验地训诲pCR率。而在另一个部队中,免疫聚首调节不仅训诲了HR+/HER2-患者的pCR率,更进一步通过MammaPrint基因检测识别出对聚首调节获益更多的超高危东说念主群。在3期临床接头CheckMate 7FL[16]和KEYNOTE-756[17]接头中,均不雅察到了新辅助化疗聚首ICI调节对pCR的训诲。咱们也期待这两项接头异日生计数据的公布,将选择咱们更多的信心,针对高危东说念主群、上风东说念主群进行更多免疫调节的尝试。
总体而言,HR阳性晚期乳腺癌的调节范围迎来了变革,跟着CDK4/6阻碍剂被纳入最新的调节指南算作推选的调节决策,大夫在调节晚期HR阳性乳腺癌时需要决定使用哪种具体的药物。大夫不错筹商中国批准的顺应症各异、药物的可及性、不良响应的解决、患者的调节史以及患者对药物的耐受性和确信性等成分,来定制化地取舍药物。这种更新赋予了大夫更大的取舍纯真性,以便更精确地得志患者的个性化调节需求。而在后CDK4/6阻碍剂期间,跟着基因检测工夫的逾越和新药的不断露馅,乳腺癌的精确诊疗正渐渐成为执行,包括ESR1、PAM等基因突变检测在内的内分泌靶向调节决策,将为国内患者带来更多获益。
注:指南本体触及阿斯利康未获批居品/顺应症,阿斯利康不推选任何未获批药品/顺应症的使用。
内行简介

方延曼 教师
贵州妇幼乳腺专科定约认真东说念主;贵阳市科普内行
中国妇幼保健协会后生委员会委员;中国妇幼保健协会乳腺保健专科委员会委员
中国光华科技基金会长江学术带乳腺定约(YBCSG)常务委员
中国接头型病院学会乳腺专科委员会委员;北京癌症防治学会乳腺癌后生委员会委员
贵州省抗癌协会乳腺癌专科委员会后生委员会第一届专科委员会副主任委员
贵州省乳腺疾病专科定约第一届常务理事
贵州省抗癌协会第一届乳腺癌专科委员会委员
精彩资讯等你来
参考文件:
[1] Howlader, N., et al. (2014). US incidence of breast cancer subtypes defined by joint hormone receptor and HER2 status. Journal of the National Cancer Institute, 106(5), dju055.
[2] Gonzalez-Angulo, A. M., Morales-Vasquez, F., & Hortobagyi, G. N. (2007). Overview of resistance to systemic therapy in patients with breast cancer. In Adv Exp Med Biol (Vol. 608, pp. 1-22).
[3] 中国抗癌协会乳腺癌诊治指南与范例 (2024简要版). (2024). 中国抗癌协会.
[4] 2024 V4 NCCN乳腺癌指南. (2024). National Comprehensive Cancer Network.
[5] Millis, S. R., et al. (2016). Ribociclib plus goserelin with hormonal therapy versus physician choice chemotherapy in premenopausal or perimenopausal patients with HR+, HER2– inoperable locally advanced or metastatic breast cancer: RIGHT choice study. JAMA Oncology, 2(12), 1565-1573.
[6] 2024 CSCO指南. (2024). 中国临床肿瘤学会.
[7] MONARCH plus: abemaciclib plus endocrine therapy in women with HR+/HER2- advanced breast cancer: the multinational randomized phase III study. (2020). Ther Adv Med Oncol. https://doi.org/10.1177/1758835920963925
[8] 李睿, 王斌, & 贾红燕. (2021). 乳腺癌调节中周期卵白依赖性激酶4/6阻碍剂耐药机制接头进展. 中华实验外科杂志, 38(4), 784-789.
[9] Elacestrant (oral selective estrogen receptor degrader) Versus Standard Endocrine Therapy for Estrogen Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: Results From the Randomized Phase III EMERALD Trial. J Clin Oncol. 2022;40(28):3246-3256. doi:10.1200/JCO.22.00338. Epub 2022 May
[10] Ekaterine Ar, et al. GS3-02 Camizestrant, a next generation oral SERD vs fulvestrant in post-menopausal women with advanced ER-positive HER2-negative breast cancer: Results of the randomized, multi-dose Phase 2 SERENA-2 trial [abstract]. San Antonio, TX. Philadelphia (PA): AACR; Cancer Res 2023;83(5 Suppl):Abstract nr GS3-02.
[11] Oliveira, M., Pominchuk, D., Nowecki, Z., et al. (2023). Camizestrant, a next generation oral SERD vs fulvestrant in post-menopausal women with advanced ER-positive HER2-negative breast cancer: results of the randomized, multi-dose Phase 2 SERENA-2 trial. Cancer Research, 83(5_Supplement), GS3-02.
[12] Sobhani, N., Roviello, G., Corona, S. P., et al. (2018). The prognostic value of PI3K mutational status in breast cancer: A meta-analysis. Journal of cellular biochemistry, 119(6), 4287–4292.
[13] Glozak, M. A., & Seto, E. (2007). Histone deacetylases and cancer. Oncogene, 26(37), 5420-5432.
[14] Jiang, Y. Z., et al. (2024). PI3K/AKT/mTOR信号通路阻碍剂调节乳腺癌临床期骗内行共鸣. 中华肿瘤杂志, 44(07).
[15] Campbell M, Yau C, Borowsky A, et al. Analysis of immune infiltrates (assessed via multiplex fluorescence immunohistochemistry) and immune gene expression signatures as predictors of response to the checkpoint inhibitor pembrolizumab in the neoadjuvant I-SPY 2 trial (Abstract PD6-08). Cancer Res. 2018;78(4)(suppl). doi: 10.1158/1538-7445.SABCS17-PD6-08.
[16] Loi S, McArthur HL, Harbeck N, et al. A phase III trial of nivolumab with neoadjuvant chemotherapy and adjuvant endocrine therapy in ER+/HER2– primary breast cancer: CheckMate 7FL. J Clin Oncol. 2020;38(suppl 15):TPS604.
doi:10.1200/JCO.2020.38.15_suppl.TPS604.
[17] Fatima Cardoso, Joyce O’Shaughnessy, et al. Phase 3 Study of Neoadjuvant Pembrolizumab or Placebo Plus Chemotherapy, Followed by Adjuvant Pembrolizumab or
Placebo Plus Endocrine Therapy for Early-Stage High-Risk ER+/HER2− Breast Cancer: KEYNOTE-756. Annals of Oncology. 2023.
审批编号:CN-145183 灵验期至:2025-10-10
材料由阿斯利康援救,仅供医疗卫生专科东说念主士参考
* 此文仅用于向医学东说念主士提供科学信息,不代表本平台不雅点
